【目次】
- 1. 光音響イメージング用のマイクロフルイディック脂質体プローブ
- 2. 腫瘍転移を模擬するためのTranswell統合型オルガノイドチップ
- 3. まとめ
マイクロ流体工学(Microfluidics)は、マイクロスケールの流体を精密に制御・操作する技術であり、チップラボ(Lab-on-a-Chip)またはマイクロ流体チップ技術とも呼ばれます。これは、生物学、化学、医学分析プロセスにおけるサンプル調製、反応、分離、検出などの基本操作ユニットを、マイクロスケールのチップ上に統合し、分析の全プロセスを自動で完了させる技術です。生物学、化学、医学など多様な分野における巨大な可能性から、生物学、化学、医学、流体工学、電子工学、材料工学、機械工学など複数の分野が融合した新たな研究領域として発展してきました。マイクロスケールの構造を持つため、マイクロ流体チップ内の流体はマクロスケールとは異なる特殊な性質を示し、独自の分析価値を有しています。さらに、マイクロ流体制御は、小型軽量、サンプルや試薬の少量使用、低消費電力、高速反応、大量並列処理、使い捨て可能など、多くの利点を有しています。
伝統的なMEMSプロセスと比較して、3Dプリント技術は超高精度と迅速な成形という独自の優位性を有し、マイクロ流体チップの3次元構造設計の制約を打破するだけでなく、小ロット生産コストを大幅に削減し、マイクロ流体チップのパーソナライズドカスタマイズと低コスト迅速生産を実現するための革新的なソリューションを提供しています。
以下では、BMF面投影マイクロステレオリソグラフィ(PμSL)3Dプリント技術を用いたマイクロ流体チップの応用事例を重点的に紹介します。
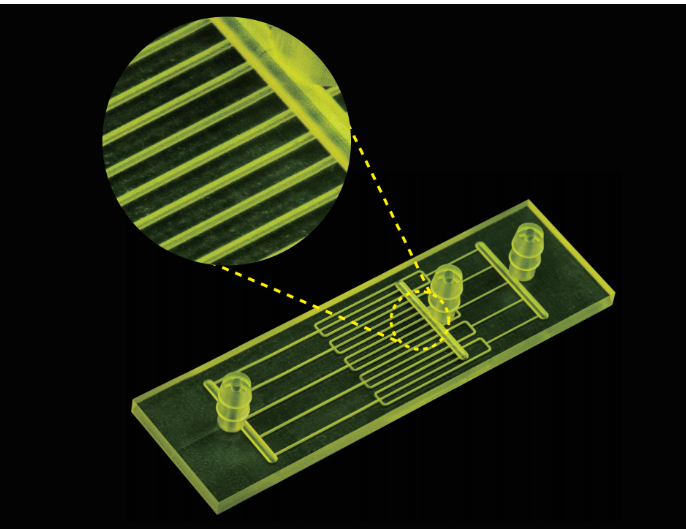
図1 BMF装置で印刷されたマイクロ流体チップ(microArch® S240)
1. 光音響イメージング用のマイクロフルイディック脂質体プローブ
光音響イメージング(Photoacoustic Imaging)は、光学イメージングの高解像度と超音波イメージングの深部組織透過能力を兼ね備えた新興の生物医学イメージング技術です。そのため、腫瘍検出、血中酸素濃度モニタリング、脳機能イメージングなど、生物医学分野において広範な応用可能性を秘めています。しかし、光音響イメージングの効果は造影剤(Contrast Agents)に大きく依存しており、造影剤を用いて光音響信号を強化することで、特定の組織や病変領域のイメージングを明確化する必要があります。
リポソーム(Liposome)は、リン脂質二重層(Lipid bilayer)から構成されるナノキャリアであり、薬剤や造影剤を負荷し、体内循環時間を延長するほか、アプタマー(Aptamers)などの表面修飾により標的送達を実現できます。従来の脂質体製造方法(溶剤注入法、薄膜水和法など)は、操作が複雑、粒径分布が不均一、改変効率が低いなどの課題を抱えています。これに対し、マイクロ流体混合技術はマイクロメートルレベルのチャンネル内で異なる液相の迅速な混合と反応を可能にし、脂質体の合成効率と均一性を大幅に向上させます。
研究内容
Zeyu Chenらはこの技術を用いてアプタマー修飾脂質体プローブを製造し、瞬時三重項差分光音響イメージング(Transient Triplet Differential-Photoacoustic, TTD-PA)に応用し、優れた標的性と高コントラストイメージング性能を示しました。
関連研究成果は「Microfluidic-enabled aptamer-modified liposomal probes for targeted transient triplet differential photoacoustic imaging」というタイトルで『Sensors and Actuators B: Chemical』誌に発表されました。
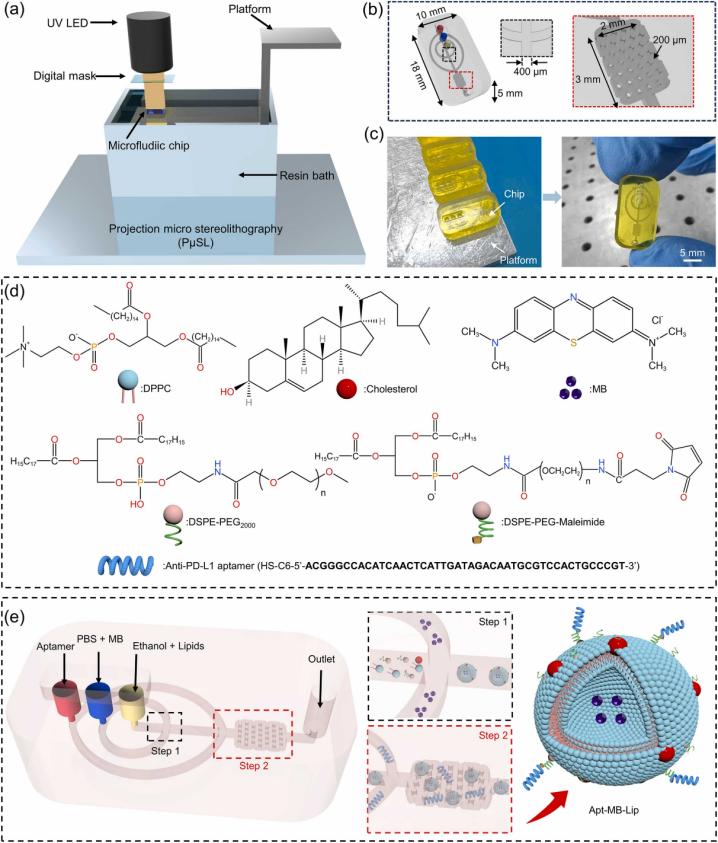
図2 微流体チップ設計、脂質体合成過程における流体混合の検証、およびApt-MB-Lipの合成模式図
まず、PμSL 3Dプリント技術(microArch® S140)を用いて、マイクロ流体チップの高効率かつ低コストでの製造を実現しました(図2(a-c)参照)。次に、マイクロ流体技術を用いて、メチレンブルー(MB)を負荷した抗PD-L1アプタマー修飾リポソーム(Apt-MB-Lip)を迅速に合成しました。このマイクロ流体チップの構造は、直径400 μmの混合チャンネル領域と直径200 μmのマイクロカラム混合領域から構成されており、この設計により、脂質体合成過程における流体の正確な制御がさらに確保され、脂質体の均一な形成とアプタマー修飾が実現されました。
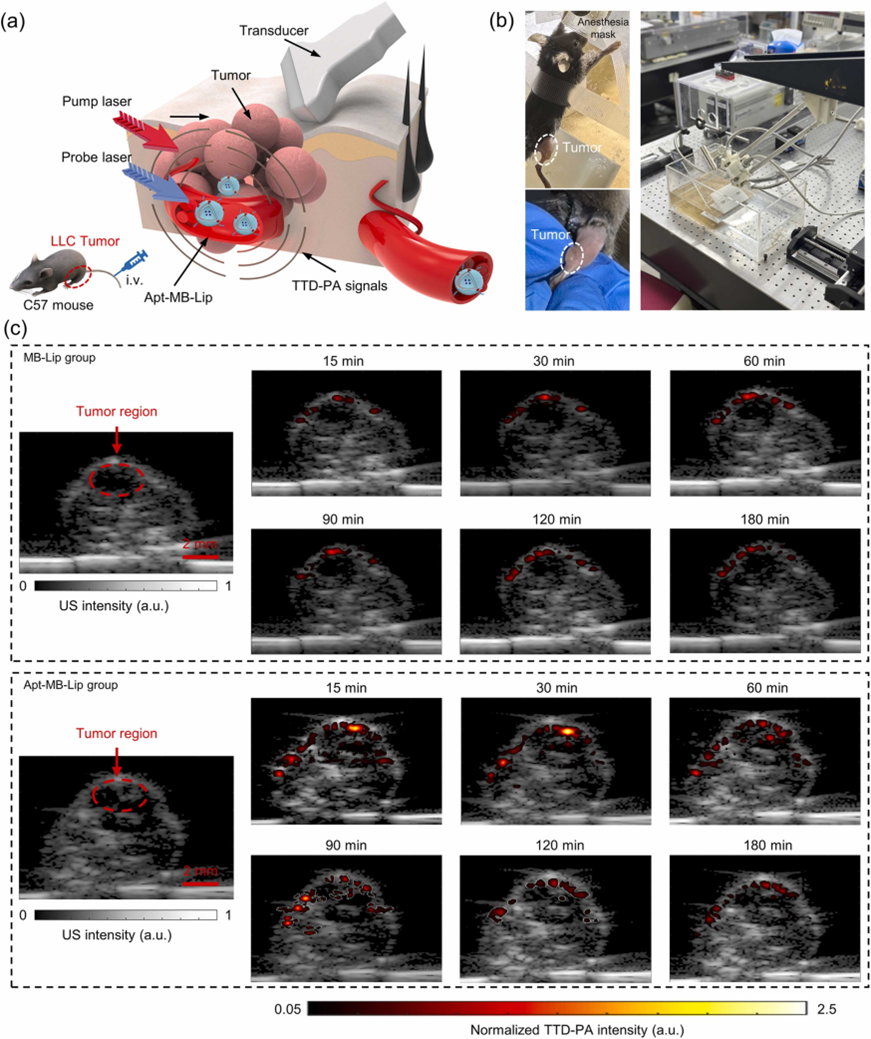
図3 体内腫瘍標的イメージング実験
その後、合成した脂質体(Apt-MB-Lip)を瞬時三重項差分光音響イメージング(TTD-PA)の体内外検証実験に用いました。体外イメージング実験では、インク、MB-Lip、およびApt-MB-Lipのイメージング効果を比較し、Apt-MB-LipがTTD-PAにおいて優れたイメージング性能を示すことが確認されました。体内イメージング実験では、Lewis肺がん(LLC)マウスモデルを使用し、MB-LipまたはApt-MB-Lipを注射後、異なる時間点でイメージングを実施しました(図3参照)。結果、Apt-MB-Lipは腫瘍領域での滞留時間が長く、信号強度も高く、優れた腫瘍標的化能力を示しました。
研究の意義
本研究では、アプタマー修飾リポソームプローブをマイクロ流体技術により調製することに成功し、その優れたターゲティング性能と一過性の三重状態差分光音響イメージングにおける高コントラストイメージング性能を実証し、がんの精密診断と標的治療のための効率的なツールを提供しました。さらに、高精度3Dプリント技術を活用することで、マイクロ流体チップは効率的かつ低コストな製造を実現するとともに、脂質体の伝統的な製造方法の限界を打破し、脂質体プローブの低コストで制御可能な製造を可能にしました。これにより、生物医学画像プローブの大量生産開発に信頼性の高い技術ソリューションを提供しています。
2. 腫瘍転移を模擬するためのTranswell統合型オルガノイドチップ
腫瘍の異質性(Tumor heterogeneity)は悪性腫瘍の特性のひとつであり、個別化医療の大きな障害となっています。腫瘍転移(tumor metastasis)は腫瘍の異質性と密接に関連しており、患者の生存率に大きな影響を及ぼします。通常、腫瘍オルガノイドは腫瘍の特性と異質性を高度に模擬し、個別化医療の新規アプローチを提供しますが、現在、有効な体外転移評価方法が不足しています。伝統的な移動実験(Transwell、スクラッチ実験など)は実際の転移プロセスを模擬できず、既存のオルガノイドチップは主に腫瘍細胞株を用いて構築されており、患者腫瘍との顕著な差異があり、臨床ニーズを満たすことが困難です。
研究内容
このため、Maike Chenらはその腫瘍転移性を評価するためのTranswell統合型オルガノイドチッププラットフォーム(Transwell-integrated organoids-on-a-chip platform、TOP)を提案しました。この腫瘍オルガノイドチップは、人体内の腫瘍の成長と転移の生理的プロセスを模倣し、患者の腫瘍細胞の浸潤能と成長能を効果的に評価できます。これにより、腫瘍の転移性に関する研究および対応する腫瘍治療と薬物研究に重要なツールを提供します。
関連研究成果は「Mimicking Tumor Metastasis Using a Transwell-Integrated Organoids On-a-Chip Platform」というタイトルで『Small』誌に発表されました。
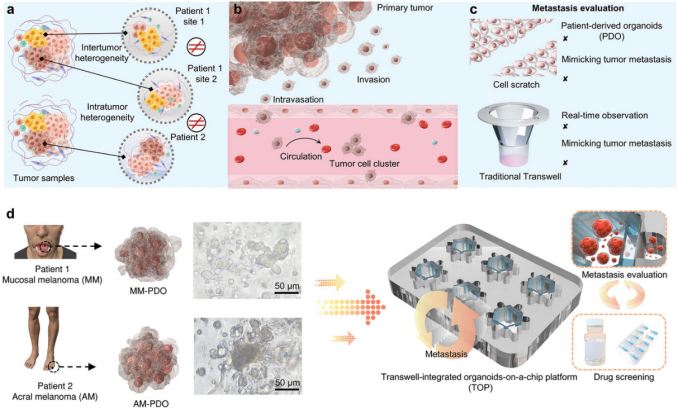
図4 Transwell統合型腫瘍オルガノイドチップを用いた腫瘍転移評価と薬剤選別
まず、レーザー切断技術を用いてポリステレン(PS)樹脂からチップ本体を製造し、次にPμSL 3Dプリント技術(microArch® S140)でチップ腔室の六角形支架を制作し、最後にTranswellユニットを統合したバイオミメティック腫瘍オルガノイドチップを完成させました(図5参照)。
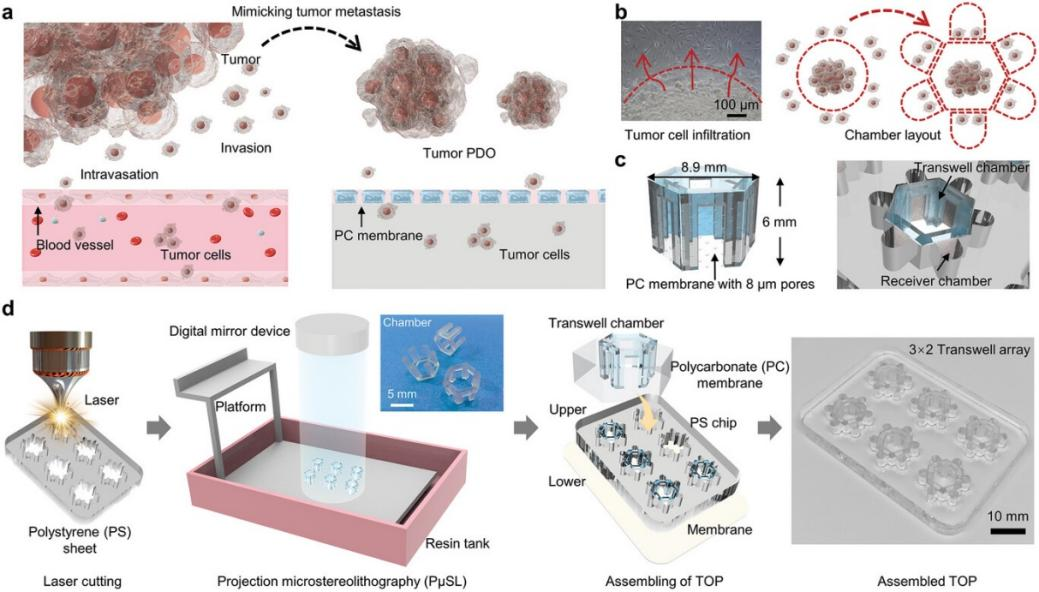
図5 生体模倣腫瘍オルガノイドチップの製造
腫瘍オルガノイドチップ内に栄養濃度勾配を構築し、外側腔室における栄養物質の濃度を中央腔室より高く設定することで、患者由来の粘膜メラノーマオルガノイド(mucosal melanoma patient-derived organoids, MM-PDO)と肢端メラノーマオルガノイド(acral melanoma patient-derived organoids, AM-PDO)の腫瘍転移能力を評価しました。観察結果から、中心腔室の腫瘍類器官が徐々に外側の腔室へ転移することが確認され、両種類のメラノーマ類器官が異なる腫瘍転移能を示すことが示されました。さらに、転移性細胞クラスターと非転移性腫瘍オルガノイドのタンパク質発現と遺伝子発現を比較したところ、転移性細胞クラスターのタンパク質発現と遺伝子発現の両方が、非転移性オルガノイドのそれよりも有意に高いことが明らかになり、この腫瘍オルガノイドマイクロアレイが腫瘍の転移を評価する能力を有することも示されました。
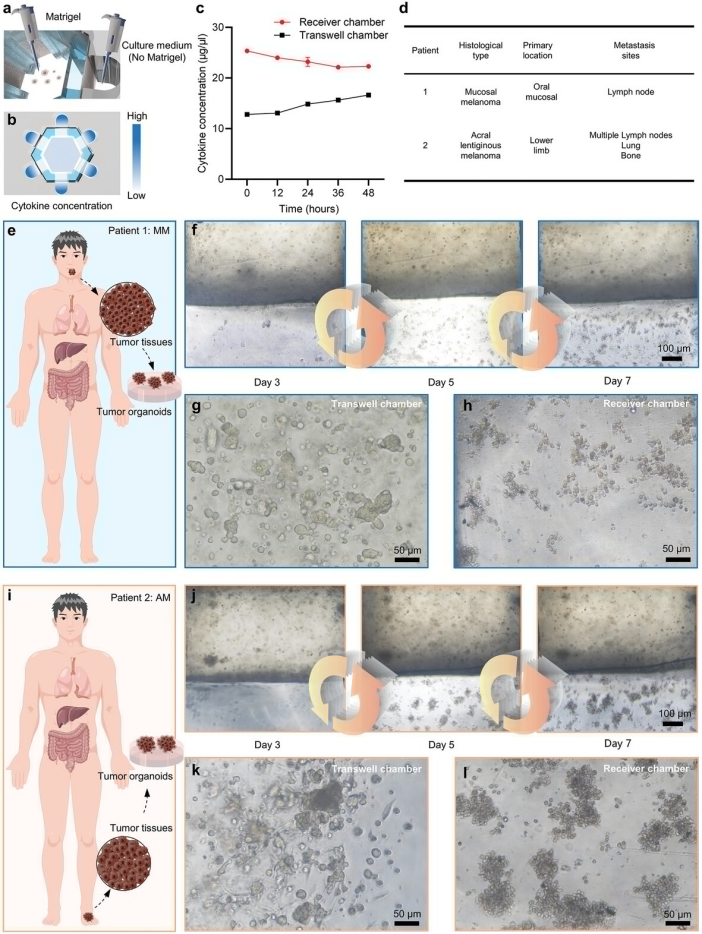
図6 腫瘍類器官チップによる腫瘍転移の評価
さらに、類器官チップ内に異なる濃度の抗腫瘍薬を追加することで、腫瘍類器官の転移性が異なることが判明し、薬物濃度が上昇するにつれ、腫瘍の転移が著しく抑制されました。したがって、この類器官チップは薬物スクリーニングプラットフォームとしても活用可能です。
研究の意義
本研究では、腫瘍転移を模擬する腫瘍類器官チッププラットフォーム(TOP)を提案しました。このプラットフォームは、腫瘍転移プロセスをより正確に模擬するだけでなく、タンパク質と遺伝子レベルで腫瘍転移を総合的に評価でき、従来のTranswell技術が腫瘍微環境と動的転移の模擬において抱えていた課題を補完しています。さらに、このプラットフォームは抗転移薬のスクリーニングにおいて大きな可能性を示しており、新規抗腫瘍療法の開発に効率的なツールを提供し、がん治療戦略の最適化と革新を促進する可能性があります。
3. まとめ
高精度PμSL 3Dプリント技術は、マイクロ流体制御分野に革命的な突破口をもたらしました。この技術は、マイクロ流体制御チップの複雑な3次元構造の効率的な製造を実現することで、臓器チップや精密医療などの革新的な応用を促進するだけでなく、マイクロ流体制御技術の発展と応用における重要な技術的基盤を提供し、工業やバイオメディカル分野などにおけるマイクロ流体制御技術の多様な応用可能性を拡大しています。







